重医附一院临床试验管理系统(CTMS)正式启用,赋能临床研究智能化、高效化、精细化管理
近日,重医附一院临床试验管理系统(CTMS)正式启用。该系统将全面赋能医院临床研究的智能化、高效化、精细化管理,为提升临床研究效率、促进医疗服务改进提供有力支持。
据悉,自2024年以来,重医附一院科研处围绕医院党委“两个聚焦、两个推动”的发展思路,通过实施一系列多维度、深层次的改革创新举措,大力推进临床研究体系和能力建设,多项工作取得了显著成效。
信息赋能——助力管理工作数字化
本次启用的CTMS系统可实现临床研究项目的全生命周期管理,覆盖项目立项、协议审核、伦理审查、访视管理、质控管理、药品管理(中心药房)、试验结题审查以及资料归档等管理模块。该系统使临床试验管理完成了从传统的人工化、纸质化管理向全面数字化管理的转变,不仅大幅提升了管理效率,更增强了数据的准确性和可追溯性,为临床研究的科学开展提供了有力支撑。
截至目前,重医附一院2024年临床研究项目承接数量和经费均创历史新高,极大地提升了该院每百名卫生技术人员科研项目经费的比例。
流程优化——提升项目开展效率
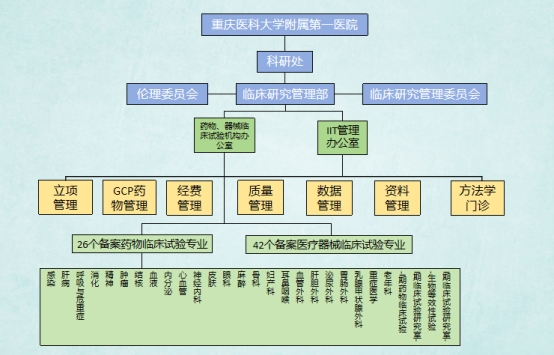
为进一步统筹管理医院临床研究工作,重医附一院科研处于今年设立了临床研究管理部,调整重组临床研究管理委员会,全面推进临床研究体系建设,有效把控临床研究管理的质量和效率,实现了“立项审查-科学审查-伦理审查-合同管理-过程管理-结题管理”的全流程管理,以及临床试验多流程并行管理。项目立项到启动的周期从原来的数月优化至1个月左右,有效提高了GCP项目的推进效率。
质量把控——保障研究科学可靠
针对在研项目,临床研究管理部质量管理人员积极开展项目质控工作,对项目立项、早期、中期和锁库前等各个重要阶段,实施全面严格的质量管理,确保每一项临床研究数据真实、准确、完整,为研究结果的有效性和安全性保驾护航。此外,临床研究管理部要求临床试验机构高度重视主要研究者的遴选流程,对新任主要研究者实施更为严格的资格审查和培训考核,以此作为规范开展项目和切实保障研究参与者权益的有力前提。截至目前,该院已有主要研究者93名,专业范畴覆盖了全院绝大部分临床医技专业,为临床试验的多元化和专业性奠定了坚实基础。
为加强研究者规范开展临床研究的意识,临床研究管理部开展了多层次、全方位的临床研究培训,并开设临床研究方法学门诊,进一步提升研究设计的科学性和研究者的临床研究能力,同时通过拟定临床研究(IIT)培育计划,全力孵育高质量临床研究。

制度保障——完善临床研究规范
完善的制度是临床研究顺利开展的基石,也是抓实研究质量与安全的重要保障。为此,临床研究管理部深入开展调研,依据国家现行法规对研究者发起的临床研究和注册类临床试验项目管理办法及经费管理办法进行了制定和修订,并出台了相应的配套管理制度和标准操作规程,让临床研究每项工作都有章可循,有据可依。

下一步,重医附一院临床研究管理部将持续开拓创新,努力构建更加完善的临床研究体系,以更高标准推进临床试验规范化建设,孵育高质量临床研究项目,提升医务人员临床研究能力,更好地发挥研究型医院的创新引领作用,为推动我国生物医药产业发展,助力健康中国建设作出贡献。
来源:科研处
编辑:姜佳妮 宁宇琪
校对:陈唯
审核:李俊龙 李丹








